
华东医药 视觉中国 资料图
添加微信好友, 获取更多信息
复制微信号
手握多款GLP-1(胰高血糖素样肽-1)药物的华东医药交出了营收净利双增的三季报。
10月24日晚间,华东医药股份有限公司(华东医药,000963)发布2024年第三季度业绩报告,前三季度营业收入314.78亿元,同比增长3.56%,归母净利润25.62亿元,同比增长17.05%,归母扣非净利润24.82亿元,同比增长14.9%。
单季度来看,第三季度营业收入105.13亿元,同比增长5.03%,归母净利润8.66亿元,同比增长14.71 %,归母扣非净利润8.57亿元,同比增长16.93%。
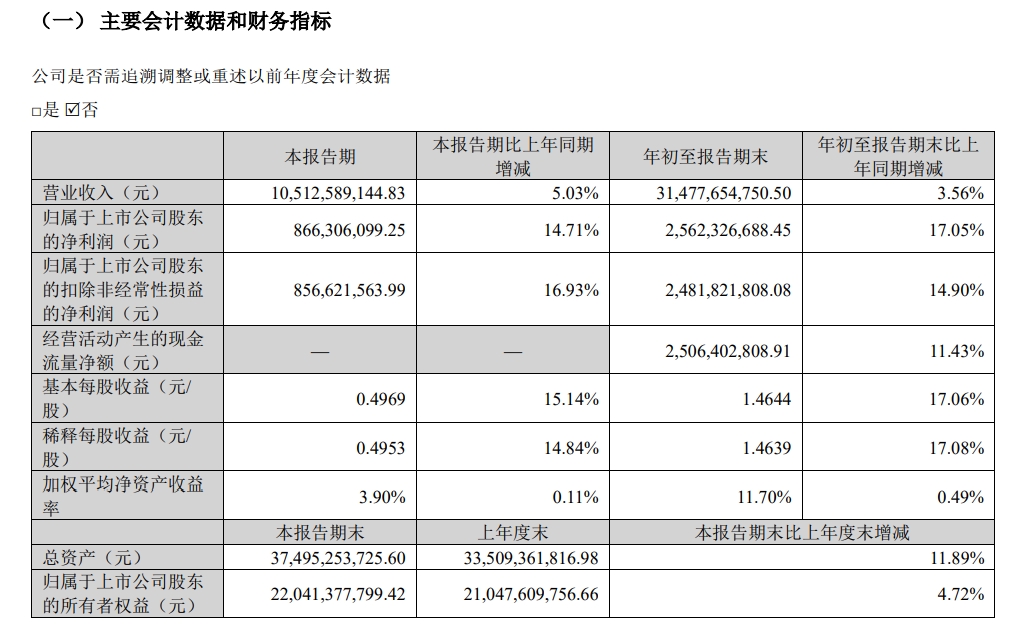
华东医药三季报数据
华东医药业务主要包括医药工业、医药商业、医美、工业微生物四大板块。商业板块贡献收入最多,前三季度营业收入205.71亿元,同比增长1.38%,累计净利润3.23亿元,同比增长2.09%。工业板块前三季度营业收入99.41亿元(含CSO业务),同比增长10.53%,归母净利润 21.4亿元,同比增长14.49%。
但华东医药被外界关注的的不少亮点都在工业板块,尤其是在内分泌领域,华东医药布局了多款大火的GLP-1药物。此前,华东医药的生物类似药利拉鲁肽已经在国内获批糖尿病、减重适应证。
目前,华东医药还在推进司美鲁肽生物类似药的研究进展。三季报提到,司美格鲁肽注射液糖尿病适应证已完成Ⅲ期临床研究全部受试者入组,预计2024年第四季度获得主要终点数据并递交pre-BLA(预生物制品上市许可申请)沟通。10月10日,华东医药曾公告称,司美格鲁肽注射液临床试验申请获得批准,同意本品按生物类似药途径开展体重管理适应证临床试验。
在GLP-1创新药方面,目前华东医药管线中有一款口服小分子GLP-1受体激动剂HDM1002。三季报显示,该药已完成用于超重或肥胖人群的体重管理适应证Ⅱ期临床研究全部入组,预计于2024年10月获得顶线结果,预计2024年第四季度进行pre-Ⅲ期沟通;同时已完成糖尿病适应证II期临床研究首例受试者入组。
此外,华东医药还有GLP-1R/GIPR 双靶点长效多肽类激动剂HDM1005,目前正在中国开展的Ia 期、Ib期临床试验进展顺利,预计于2024年第四季度获得Ia期临床研究报告、Ib期(第一部分)临床试验的顶线结果,并计划于2025年初启动II期临床试验;控股子公司浙江道尔生物科技有限公司在研的FGF21R/GCG/GLP-1靶点的多重激动剂DR10624目前正在新西兰开展肥胖合并高甘油三酯血症的Ⅰb/Ⅱa期临床试验;同时,重度高甘油三酯血症的国内II期临床已启动,目前已完成首例受试者入组及给药。
在医美板块,华东医药前三季度营业收入19.09亿元(剔除内部抵消因素),同比增长1.9%。其中国内医美全资子公司欣可丽美学营业收入9.09亿元,同比增长10.31%。
近期,华东医药在医美板块的一起官司同样受到行业关注。10月11日,华东医药(000963.SZ)旗下“伊妍仕”公众号发布诉讼声明,称一款国产“少女针”侵犯自身发明专利权。
根据声明,华东医药子公司欣可丽美学于近日向上海知识产权法院就被告山东采采医疗科技有限公司、山东谷雨春生物科技有限公司、山东采采医疗科技有限公司上海第一分公司就其注射用聚己内酯微球面部填充剂商业化行为侵害发明专利权纠纷一案提起民事诉讼,上海知识产权法院已于10月10日正式受理,并于近日向欣可丽美学送达了《案件受理通知书》。
对此,谷雨春及子公司采采医疗10月11日也发布回复声明称,不存在任何侵犯专利权利的行为。截至发声明之日,公司未收到任何法院关于侵害发明专利纠纷诉讼的传票、应诉通知书以及举证的通知书等材料。如收到,公司将严肃应对,维护公司正当权益。
10月24日收盘,华东医药报33.78元/股,跌0.35%,市值592.6亿元。












还没有评论,来说两句吧...